Cell主刊:高內(nèi)涵篩選助力攻克毒性蛋白質(zhì)病難題

毒性蛋白質(zhì)病(Proteinopathy)通常由細(xì)胞內(nèi)或細(xì)胞外沉積大量折疊變異的蛋白質(zhì)(Misfolded protein)所致。在蛋白合成和成熟過程中的任何一個環(huán)節(jié)出現(xiàn)問題,如蛋白突變、折疊以及翻譯后修飾出現(xiàn)異常都有可能會導(dǎo)致蛋白質(zhì)病的發(fā)生。雖然蛋白質(zhì)病這個術(shù)語對很多人來說還比較陌生,但現(xiàn)已證明其和多種嚴(yán)重的神經(jīng)性疾病,如阿爾茲海默癥、帕金森病和肌萎縮性側(cè)索硬化癥(ALS)的發(fā)生密切相關(guān)。靶向蛋白質(zhì)病的研究也為屢屢受挫的神經(jīng)退行性疾病治療提供了新的曙光[1,2]。
高內(nèi)涵整體解決方案的優(yōu)異體現(xiàn)
在七月的Cell主刊中,研究將目光轉(zhuǎn)至由MUC1基因移碼突變導(dǎo)致的腎病(MUC1 kidney disease ,MKD)[3]。與神經(jīng)性退行性疾病類似,MKD目前尚無有效治療手段。結(jié)合細(xì)胞系、小鼠模型、病人組織和日益火熱的類器官來源樣本,研究證實MUC1突變蛋白(MUC1-fs)會大量聚集在細(xì)胞內(nèi),并最終激活未折疊蛋白應(yīng)答(Unfolded protein response UPR),誘發(fā)細(xì)胞損傷和毒性。因此,MKD也屬于蛋白質(zhì)病的一種。針對該發(fā)病機(jī)制,研究實施基于高內(nèi)涵平臺的高通量篩選,并成功獲得能特異清除突變MUC1蛋白的小分子藥物BRD4780。該研究不僅深入我們對蛋白轉(zhuǎn)運異常發(fā)生機(jī)制的了解,也為多種毒性蛋白質(zhì)病提供了新的治療策略和切入點。在七月的研究熱點版塊中,Nature Review Drug Discovery專門針對發(fā)現(xiàn)進(jìn)行了解析[4]。
該研究也體現(xiàn)了珀金埃爾默高內(nèi)涵整體解決方案的高效應(yīng)用。成像平臺Opera Phenix配合CellCarrier Ultra系列微孔板主導(dǎo)高內(nèi)涵篩選的同時,并通過水鏡優(yōu)勢參與了基于上述四種樣本的所有熒光拍攝和動態(tài)追蹤分析細(xì)胞凋亡進(jìn)程。針對類器官樣本的拍攝,PreciScan功能被用于提速拍攝進(jìn)程和排除不需要的圖像采集和分析。所有的熒光分析由Harmony軟件完成,尤其是‘spot’分析功能的應(yīng)用。

a疾病解析
通過MKD病人和體外模型等樣本,研究使用抗體染色方式分析野生型MUC1和對應(yīng)突變產(chǎn)物的組織和細(xì)胞分布。在不同來源的樣本中,值得一提的是基于病人誘導(dǎo)性多能干細(xì)胞(induced pluripotent stem cells , iPS cells)建立的類器官(Organoid)樣本。基于干細(xì)胞技術(shù)的類器官模型建立和分析也是近年來高內(nèi)涵的優(yōu)勢應(yīng)用方向之一[5]。與病人的切片結(jié)果一致,野生型MUC1主要分布在類器官的頂膜部位,而突變蛋白則分布在細(xì)胞內(nèi)。進(jìn)一步研究證明聚集在細(xì)胞內(nèi)的突變MUC1會誘發(fā)細(xì)胞應(yīng)激,活化ATF6-UPR通路并最終導(dǎo)致細(xì)胞損傷,表明MKD是蛋白質(zhì)病。
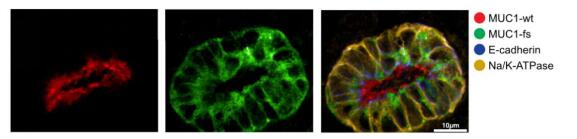
基于MKD病人的腎類器官模型染色,圖片由Opera Phenix拍攝。
紅色指示野生型MUC1蛋白;綠色指示突變體MUC1蛋白;藍(lán)色為E-cadherin;黃色為Na/K ATPase標(biāo)記基底外側(cè)膜。
b高內(nèi)涵篩選
為了發(fā)現(xiàn)能有效清除突變蛋白的藥物,研究針對病人樣本建立永生化細(xì)胞系,并利用Opera Phenix開展大規(guī)模、多指標(biāo)高內(nèi)涵篩選。在初篩中,研究關(guān)注能清除突變蛋白并無顯著細(xì)胞毒性的藥物,并在此基礎(chǔ)上細(xì)化篩選藥物濃度開展二輪篩選。通過兩輪篩選后,研究通過特異性、mRNA水平調(diào)控和是否能抑制ER應(yīng)激藥物thapsigargin的細(xì)胞毒性三個指標(biāo)來進(jìn)一步分析候選藥物。
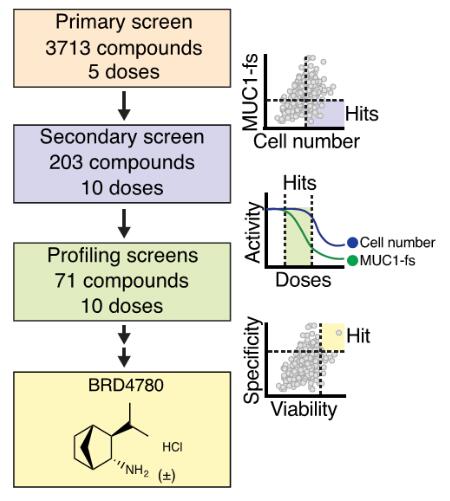
高內(nèi)涵篩選流程圖
最終,從3713種化合物中,研究成功發(fā)現(xiàn)BRD4780滿足上述的指標(biāo),能有效特異清除突變蛋白的同時不影響MUC1轉(zhuǎn)錄水平,并能保護(hù)病人模型細(xì)胞系不受thapsigargin的應(yīng)激壓力。進(jìn)一步的實驗證明BRD4780能工作于類器官模型和小鼠模型,是非常有潛力的MKD治療藥物。
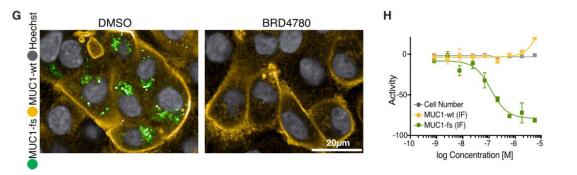
左圖:基于細(xì)胞系的染色結(jié)果,黃色指示野生型MUC1蛋白;綠色指示突變體MUC1蛋白;灰色指示細(xì)胞核。
右圖:對應(yīng)的統(tǒng)計分析和細(xì)胞數(shù)變化分析。
c機(jī)制研究
為了解析MUC1突變體亞細(xì)胞聚集原理和BRD4780工作機(jī)制,研究利用成像技術(shù)進(jìn)行大量共定位研究,并發(fā)現(xiàn)病人來源細(xì)胞系中MUC1突變體滯留在內(nèi)質(zhì)網(wǎng)和高爾基體之間的早期分泌通路中,并與運貨受體TMED9有顯著的共定位趨勢,且這個現(xiàn)象能進(jìn)一步在多種模型和病人組織中重現(xiàn)。通過動態(tài)成像追蹤,研究證明BRD4780能將滯留的突變蛋白從早期分泌途徑中釋放出來,并促進(jìn)其進(jìn)入溶酶體降解途徑。

基于細(xì)胞系的亞細(xì)胞共定位研究,分析基于Harmony軟件的‘spot’ 分析功能。

基于細(xì)胞系、小鼠模型、病人組織和類器官來源樣本的熒光染色分析,紅色指示TMED9;綠色指示突變體MUC1蛋白;灰色指示細(xì)胞核。
* 熒光圖片均由Opera phenix 拍攝。
非常有意思的是,在病人樣本中研究同時也發(fā)現(xiàn)TMED9蛋白水平的上升,而BRD4780處理同樣能降低TMED9蛋白水平。此外,通過CRISPR技術(shù)敲除TMED9能表型模擬BRD4780的處理效果,清除突變蛋白。因此,TMED9參與了MUC1突變體在早期分泌途徑的滯留和積累,并可能是BRD4780的直接作用靶點。針對此,研究采取細(xì)胞熱移位測定法(Cellular thermal shift assay,CETSA)證實細(xì)胞內(nèi)BRD4708和TMED9存在直接相互作用。憑借其能在生理條件下進(jìn)行細(xì)胞水平分析的優(yōu)勢,CETSA成為了內(nèi)源蛋白-藥物相互作用分析技術(shù)的生力軍,是表性篩選下游藥物解析的利器。
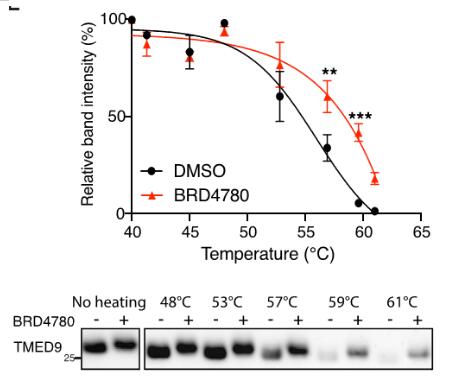
基于CETSA方法在細(xì)胞水平確認(rèn)BRD4708能直接結(jié)合TMED9
綜合上述的發(fā)現(xiàn),研究向我們闡釋了MKD的發(fā)病以及BRD4780的作用機(jī)制。通過直接結(jié)合TMED9,BRD4780將突變的MUC1蛋白從內(nèi)質(zhì)網(wǎng)和高爾基體之間的早期分泌通路中釋放出來,加速溶酶體對其的清除。令人興奮的是,在具有很好的藥理性質(zhì)的同時,BRD4780不僅能作用于MKD,還能作用于其他多種膜相關(guān)蛋白導(dǎo)致的毒性蛋白質(zhì)病,如UMOD突變相關(guān)的慢性腎病和色素性視網(wǎng)膜炎等,是非常有潛力的候選藥物。

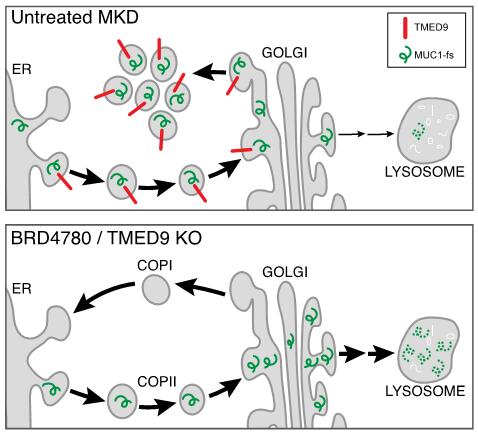
MKD的發(fā)病機(jī)制和BRD4780的作用機(jī)制圖
同時,該研究也是高內(nèi)涵兩大應(yīng)用領(lǐng)域的精華案例。首先是亞細(xì)胞水平成像應(yīng)用,研究中涉及到的大量定位、共定位研究和動態(tài)追蹤蛋白轉(zhuǎn)運過程都是高內(nèi)涵的優(yōu)勢應(yīng)用場景。其次,更為關(guān)鍵的是,該研究也是成像篩選主導(dǎo)的藥物發(fā)現(xiàn)案例。從疾病模型表型的建立到靶向逆轉(zhuǎn)疾病相關(guān)表型的篩選,和最后下游的藥物機(jī)制研究,都離不開珀金埃爾默高內(nèi)涵解決方案。高內(nèi)涵解決方案,伴隨著機(jī)器學(xué)習(xí)的逐漸成熟,將成為創(chuàng)新藥物研發(fā)行業(yè)的新鮮血液[6]。
參考文獻(xiàn)
1. Ganguly G, et al.Proteinopathy, oxidative stress and mitochondrial dysfunction: cross talk in Alzheimer's disease and Parkinson's disease. Drug Des Devel Ther. 2017 Mar 16;11:797-810.
2. Scotter EL, et al.TDP-43 Proteinopathy and ALS: Insights into Disease Mechanisms and Therapeutic Targets. Neurotherapeutics. 2015 Apr;12(2):352-63. doi: 10.1007/s13311-015-0338-x.
3. Dvela-Levitt M, et al.Small Molecule Targets TMED9 and Promotes Lysosomal Degradation to Reverse Proteinopathy. Cell. 2019 Jul 25;178(3):521-535.e23.
4. A novel approach to reverse proteinopathies https://www.nature.com/articles/d41573-019-00133-5
5. Czerniecki SM, et al.High-Throughput ScreeningEnhancesKidneyOrganoid Differentiation from HumanPluripotent Stem Cells and Enables Automated Multidimensional Phenotyping. Cell Stem Cell. 2018 Jun 1;22(6):929-940.e4.
6. Machine learning brings cell imaging promises into focus https://www.nature.com/articles/d41573-019-00144-2
關(guān)于珀金埃爾默:
珀金埃爾默致力于為創(chuàng)建更健康的世界而持續(xù)創(chuàng)新。我們?yōu)樵\斷、生命科學(xué)、食品及應(yīng)用市場推出獨特的解決方案,助力科學(xué)家、研究人員和臨床醫(yī)生解決最棘手的科學(xué)和醫(yī)療難題。憑借深厚的市場了解和技術(shù)專長,我們助力客戶更早地獲得更準(zhǔn)確的洞見。在全球,我們擁有12500名專業(yè)技術(shù)人員,服務(wù)于150多個國家,時刻專注于幫助客戶打造更健康的家庭,改善人類生活質(zhì)量。2018年,珀金埃爾默年營收達(dá)到約28億美元,為標(biāo)準(zhǔn)普爾500指數(shù)中的一員,紐交所上市代號1-877-PKI-NYSE。了解更多有關(guān)珀金埃爾默的信息,請訪問www.perkinelmer.com.cn。
標(biāo)簽:
高內(nèi)涵篩選
Copyright(C) 1998-2024 生物器材網(wǎng) 電話:021-64166852;13621656896 E-mail:info@bio-equip.com