��ǰλ�� > ��� > ���g(sh��)���� > IVISҕ�ǣ����I�������[���ί��I(l��ng)��đ�(y��ng)��
IVISҕ�ǣ����I�������[���ί��I(l��ng)��đ�(y��ng)��
IVISҕ�ǣ����I������Щ�������������I�������[���ί��I(l��ng)��đ�(y��ng)��
�[�����w��(n��i)ֻ��һ��Ŀ�������Dz�ͣ�����L�����L�����L�������L���^���в��ɱ����Ҫ���ĵ�����������͠I�B(y��ng)���|(zh��)�������[������(g��u)��������Ѫ�ܾW(w��ng)�j(lu��)ϵ�y(t��ng)�����B(y��ng)�ֺ������ݔ�ͣ��@Щ�[����(n��i)�����Ѫ�ܾ����[������������(y��ng)վ������Д��[�������ӠI�B(y��ng)����(y��ng)���Ɖ��[�����������xϵ�y(t��ng)�����������[����������ֳ���Ķ����I������������
�������@�N�����Д�ǏV�x�ϵ����˜p���Mʳ�������ٳԠI�B(y��ng)�Ė|�����@�ӕ�ʹ�����M���ò�������������(d��o)���������½������������I���������x���ԣ������خ��Ե������[�������Ĵ��x�^�̣��D1�������F(xi��n)���[���ľ������������

�D1 �خ��������[�������������x
��(li��n)�{��ø�����[�������I���h(hu��n)��
ͨ�^��(li��n)�{�״�ˎ����O(sh��)Ӌ��������������ø(GOx)���^������ø(CAT)ͨ�^pH푑�(y��ng)�ľۺ��サ(li��n)�γɼ�(li��n)�{��ø��ͨ�^Ѫ�嵰���{��ø�Ϳ��[��ǰˎ��(f��)���γɼ{��ˎ��[�������ԭh(hu��n)�����Ԍ��{��øጷ���COxѸ�������[��������(n��i)�������Ǻ��������a(ch��n)�����I��ȱ���h(hu��n)�����Д��[����������(y��ng)��ͬ�r����ǰˎϵ�y(t��ng)�Ļ��W(xu��)�ί�Ч�����������������Ǯa(ch��n)���Ķ����a(ch��n)��H2O2Ҳ���Կ��ٱ�CAT�ֽ����Ա���a(ch��n)��ȫ�����ԡ��@�N�Y(ji��)�ϰ������I�h(hu��n)�����Y(ji��)��ȱ�����W(xu��)�ί��ķ���������Ч�����[����������ֳ�������a(ch��n)���������ã�ͨ�^С�����W(xu��)�����������Ŀ�����(li��n)�{��ø�w�����[����λ�ĸ����S�r�g��׃����r���Լ�48С�r��{��ø�w���ڸ����K���еķֲ���r��
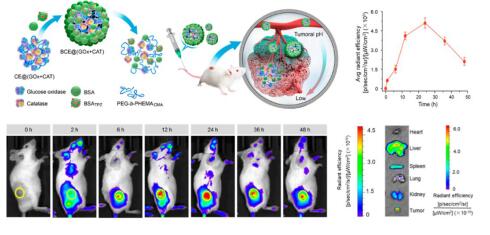
�D2 ���ڼ�(li��n)�{��ø�ļ{��ˎ���O(sh��)Ӌ�Լ����w��(n��i)�İ���ֲ���r
�����īI
Ma Y, Zhao Y, Bejjanki N K, et al. Nanoclustered Cascaded Enzymes for Targeted Tumor Starvation and Deoxygenation-Activated Chemotherapy without Systemic Toxicity[J]. ACS nano, 2019, 13(8): 8890-8902.
�����T��(d��o)�[���������x���
ͨ�^���ͼ{���w���Ę�(g��u)���������[�������߱��_�M������øB���������O(sh��)Ӌø�����_�P(gu��n)�����d�й��Ľ�{��ͺͶ�λ������������u�w��ż(li��n)��һ���γ�����-�l(w��i)�ǽY(ji��)��(g��u)�����[�������zȡ��{���w�����Ա��߱��_�ĽM������øB���У�����-�l(w��i)�ǽY(ji��)��(g��u)���_����ϲ�ͬ���εĹ���ͬ�r���l(f��)��������Ч��(y��ng)���Д��[���������ữ���ǽͽ��^���������������(y��ng)�������[������ֳ��ͨ�^С������w��W(xu��)�����M�иβ��D(zhu��n)���[�����w��(n��i)���������Y(ji��)�������@�N�{���w����Ϲ��տ�����Ч�T��(d��o)�[�������a(ch��n)�������I���h(hu��n)����ͨ�^�����[��������������(y��ng)����w��(n��i)���D(zhu��n)���[����������������(n��i)�M������øB��������������-�l(w��i)�ǽY(ji��)��(g��u)�o�����_���ڹ����^���й�����a(ch��n)���Ćξ��B(t��i)�������Mһ�������{�������u�w������K��ᷴ��(y��ng)�İl(f��)��������Ӱ푵������M���Ĵ��x�^�����C���˿��Ի����������x���[���x���Ծ����ί����ԵĿ�������
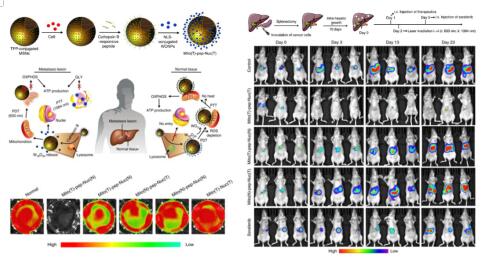
�D3 �������[��������������(y��ng)
�����īI
Huo D, Zhu J, Chen G, et al. Eradication of unresectable liver metastasis through induction of tumour specific energy depletion[J]. Nature communications, 2019, 10(1): 1-17.
�˺���
�[��
- �о��Mչ��ҕ�l����(d��o)���ֳ�ʽ���ٹ�W(xu��)��Ɍ�������ϵ�y(t��ng)
- ULTIMUS 9 LABС���ﳬ�ֱ泬����ϵ�y(t��ng)�a(ch��n)Ʒ���g(sh��)��(y��ng)�ÄӑB(t��i)
- �������Ͷ���V�̲��t������u�����w������(chu��ng)������
- ��W(xu��)��Ɍ�������OCT����N������չ���Է���
- ������ο���ӛ�R���[���ӱ����Ƚ��t��Ͷ̲��t�����Ч��
- ͨ�^Au-Se�I�˷���{���w���ĸ��K�����D(zhu��n)���ϵK�������w��(n��i)������
- �ǽ��|ʽ�̲��t����������]���µĄӑB(t��i)����ͫ�לy������ҕ�u��
- ���ö̲��t������ɢ�䌍�F(xi��n)���^�o��ӛ�������t(y��)�W(xu��)����
- �M���Y��������ӵ�����ȫ�����R�~PI���
- �����v������w�����И������䰲������W(xu��)�t(y��)�W(xu��)Ժ
- �����v����(n��i)��չʾ�����������t(y��)�W(xu��)�ƌW(xu��)Ժʢ�����
- �W�����F�y�_ʽ��CT�ȃx����������2024�Ϻ�QCչ��
- �����v�����ɹ�̽ᘰl(f��)չ�c��(y��ng)������߷�Փ���������
- ���ʺ�I(y��)�w���ZС���ﳬ����ϵ�y(t��ng)�ɹ�����ձ��Ј�
- �_���������Ї�ѭ�h(hu��n)�W(xu��)����11��ȫ��ѭ�h(hu��n)���
- ף�R���Jҕ�Ƽ��c�|�A��W(xu��)Micro-CT(li��n)�ό���ҳ���
Copyright(C) 1998-2024 �������ľW(w��ng) �Ԓ��021-64166852;13621656896 E-mail��info@bio-equip.com